文献分享:仪器小组
Nature: 基于化合物规模化再利用研发SARS-CoV-2抗病毒药物
Discovery of SARS-CoV-2 antiviral drugs through large-scale compound repurposing
Laura Riva, Shuofeng Yuan, Xin Yin, Laura Martin-Sancho, Naoko Matsunaga, Lars Pache, Sebastian Burgstaller-Muehlbacher, Paul D. De Jesus, Peter Teriete, Mitchell V. Hull, Max W. Chang, Jasper Fuk-Woo Chan, Jianli Cao, Vincent Kwok-Man Poon, Kristina M. Herbert, Kuoyuan Cheng, Tu-Trinh H. Nguyen, Andrey Rubanov, Yuan Pu, Courtney Nguyen, Angela Choi, Raveen Rathnasinghe, Michael Schotsaert, Lisa Miorin, Marion Dejosez, Thomas P. Zwaka, Ko-Yung Sit, Luis Martinez-Sobrido, Wen-Chun Liu, Kris M. White, Mackenzie E. Chapman, Emma K. Lendy, Richard J. Glynne, Randy Albrecht, Eytan Ruppin, Andrew D. Mesecar, Jeffrey R. Johnson, Christopher Benner, Ren Sun, Peter G. Schultz, Andrew I. Su, Adolfo García-Sastre, Arnab K. Chatterjee, Kwok-Yung Yuen & Sumit K. Chanda
前言
新冠肺炎(COVID-19)疫情暴发后,在全球迅速传播开来。截至目前,全球累计确诊的新冠肺炎病例已超1660万,累计死亡病例超65万。疫情还在持续蔓延,研发疫苗迫在眉睫。然而新冠肺炎疫苗的研制至少还需要12至18个月,并且新的治疗药物开发则需要10到17年之久。因此,针对像新冠肺炎这样新兴的传染病,快速检测并给出治疗方法是必要的,而利用经过临床评估的药物进行诊断与治疗是缩短药物开发周期的可行的策略之一。结合数据分析方法对已知药物的无偏见、大规模的评估则是实行这一策略的重要手段。
近日,桑福德-伯纳姆-普利贝斯医学研究所分析了一个包含约12000个小分子的已知药物库ReFRAME,他们发现100种分子可以抑制病毒的复制,其中包括21种药物表现出剂量-疗效关系的已知药物,且有13种药物的有效浓度可能与疾病治疗剂量相当。该研究有助于确定意想不到的治疗选择,而这些选择可能大大加速临床前和临床评估,协助制定新冠肺炎的新疗法。
内容
桑福德-伯纳姆-普利贝斯医学发现研究所(下文简称:该所)对已知药物库ReFRAME的筛查,发现了100种已知药物分子,在哺乳动物细胞中可以抑制新冠肺炎病毒的复制,包括21种可以建立与抗病毒活性呈剂量反应关系的化合物。针对这些疗法,对体内抗病毒功效的快速实验和临床评估,以及改善与疾病相关的病理可为加速开发新冠肺炎(文章中命名为SARS-CoV-2)潜在疗法的提供重要机会。
1. 对病毒复制抑制剂的高通量筛选优化
该所开发了一种高通量检测方法,可以对已知药物进行大规模筛选。选取一种源自非洲绿猴的肾脏上皮细胞Vero E6,它被证实高度允许SARS-CoV-2感染,通过测量病毒诱导的细胞病变效应(cytopathic effects, CPE)可评估病毒复制。基于测量384孔格式的病毒诱导的CPE,在细胞Vero E6中优化了鉴定参数,包括细胞接种密度,感染复数(MOI)和时间点。为了评估高通量筛选(HTS)配置中优化测定的鲁棒性和可重复性,该研究首先利用已知生物活性分子库(LOPAC®1280)评估了鉴定,并确认了PIKfyve激酶抑制剂APY0201对SARS-CoV-2潜在抗病毒活性(图1a)。这样就可以基于可靠的阳性对照对鉴定的动态范围进行基准测试。每个孔的新冠病毒诱导的CPE活性对应于标准化的每个平板的中位数(Log2FC)。筛选的平均因子Z定为0.4,(相当于Log2FC的值大于这个值,就判定为有效),相关系数(R2)为0.86(如图1b-c),取得了良好效果。根据对病毒增值的抑制活性,选择了28种化合物进行进一步确认(如图1b,APY0201组))。
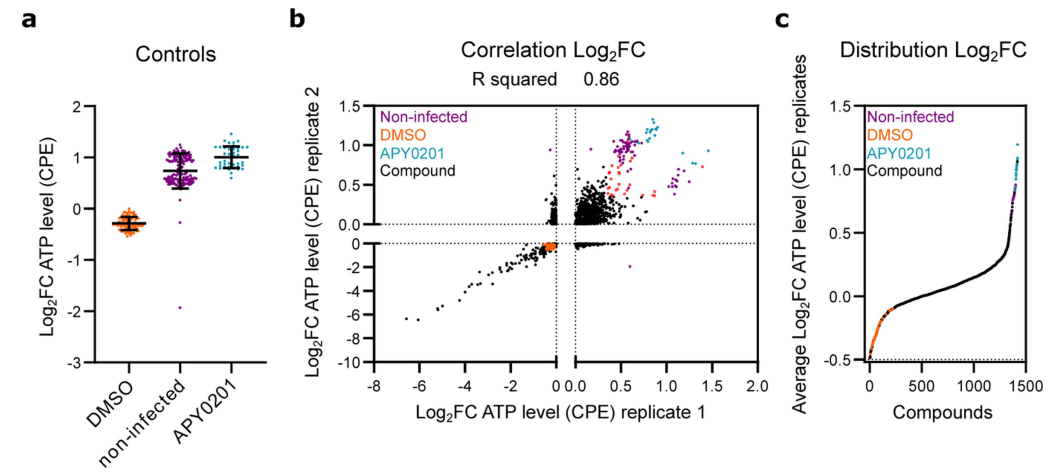
图1:用于SARS-CoV-2抗病毒药物的高通量重排筛选--来自LOPAC®1280库初步筛选的数据。a:对于SARS-CoV-2感染的所有阳性(APY0201)和阴性(DMSO)对照组,以及非感染细胞,在所有筛选板中,归一化后的ATP水平Log2 倍数变化(Log2FC)。误差条表示n=40的平均值±标准差;b: 相关图显示两个重复筛选中每个化合物的Log2FC;c:根据每个病毒增值物的Log2FC平均值,每种化合物的活性分布。
2. ReFRAME药物再利用库的重新定位分析
在确定这些测定条件适合于大规模筛选后,该所使用上述实验设计全面筛选了ReFRAME库中药物(图2a)。具体研究步骤如下:在细胞Vero E6中评估了11,987种化合物对SARS-CoV-2的潜在抗病毒活性。基于低病毒输入(MOI = 0.01)和延长的终点测量值(感染后72小时),设计了以5 µM最终化合物浓度进行的鉴定,以捕获多周期重复。观察到阳性对照和阴性对照之间的合理动态范围(图2b,2d)和重复之间存在的正相关(图2c),从而鉴定具有潜在抗病毒活性的化合物。紧接着,研究者在筛选数据中评估了已知靶标和靶标类别的丰富性。他们利用基因集富集分析(GSEA)工具,检查了化合物在单个靶标类中的抗病毒活性分布,以确定某些治疗机制是否含有比偶然预期更多的活性化合物,评估结果显示15个靶标类别中的51个药物靶标在命中列表中实现富集,这说明这些药物具有潜在疗效(图2a)。
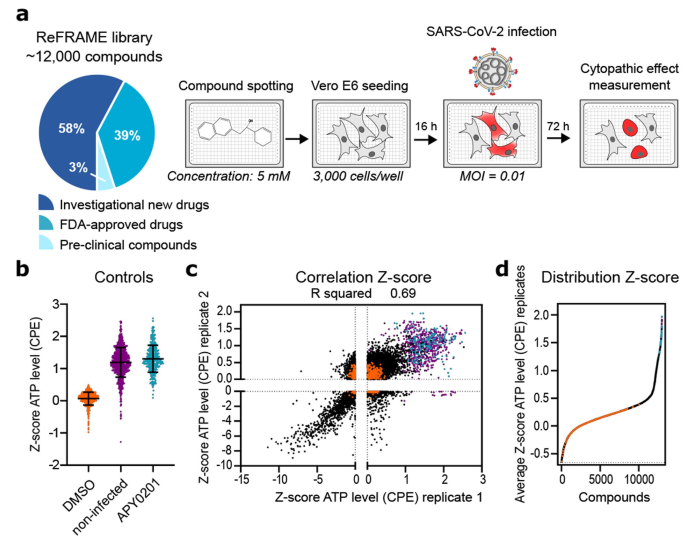
图2:用于SARS-CoV-2抗病毒药物的高通量重排筛选--来自ReFRAME库初步筛选的数据。a:用于ReFRAME库重新定位分析的筛选策略示意图。b:对于SARS-CoV-2感染的所有阳性(APY0201)和阴性(DMSO)对照组,以及非感染细胞,在所有筛选板中,归一化后ATP水平的Log2 倍数变化 (Log2FC),即Z值。误差条表示n=375的平均值±标准差;c: 相关图表明在两次重复筛选中每种化合物的活性(Z值);d:根据每个重复的z值的平均值,每种化合物的活性分布。
3. 对筛选出的抗SARS-CoV-2的化合物进行正交验证[1]
研究者选用大约300种化合物用于验证研究,使用正交测定读数,以2.5和1 µM的浓度评估了选定命中物的活性,低于原始筛选中使用的5 µM浓度。具体而言,用另一种SARS-CoV-2分离株(SARS-CoV-2 USA-WA1 / 2020)攻击用选定化合物处理过的细胞Vero E6,并通过对病毒编码的NP蛋白进行免疫染色直接量化病毒感染。发现约百分之三十的化合物(100种化合物)可减少至少40%的病毒复制。
通过验证的化合物是GSEA靶标类别的成员(图3),例如包括视黄酸受体激动剂(retinoic acid receptor agonists )(LGD-1550,维甲酸(tretinoin),他米巴罗汀(tamibarotene),阿维A(acitretin),他扎罗汀(tazarotene),RBAD),醛糖还原酶(aldose reductase)抑制剂AL 3152,苯并二氮杂受体激动剂(ZK-93426,扎来普隆GR (zaleplon GR),帕戈隆(pagoclone))和抗疟疾药物(AQ-13和hanfangchin A)。此外,在美国或日本有六种获得监管部门批准的药物属于证实可抑制SARS-CoV-2复制的分子。这些药物包括抗疟疾药物氯喹,抗银屑病分子阿维A和抗组胺阿司咪唑。
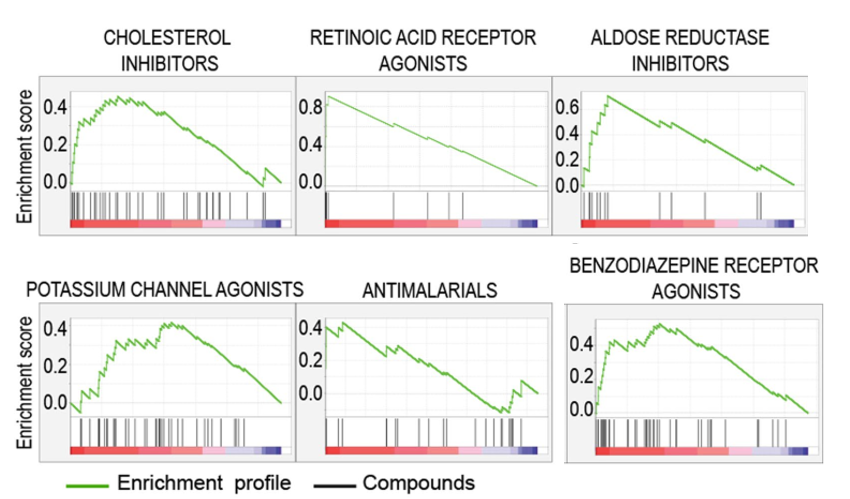
图3:基因集富集分析(GSEA)和靶标基因表达:几种经过验证的化合物是GSEA靶标类别的成员。
4. 量效关系和药物协同作用分析
尽管药物疗效高度依赖于化合物的药物代谢动力学特性,但通常预期治疗剂量范围可通过追踪低于1 µM浓度的细胞EC50(半最大效应浓度:药物安全性指标)来判定。由此,研究者对此种手段进行了剂量反应分析,以确定化合物浓度与抗病毒活性之间的关系(图4a-b)。除瑞德西韦外,还有20种化合物具有明显的剂量依赖性抗病毒活性,其中大多数可以根据广泛的功能,结构或靶标类别进行分离(图4a-b)。重要的是,细胞毒性和抗病毒活性之间存在显着差异(图4a),强调这些化合物对病毒复制的影响远超出分子的细胞毒性或细胞抑制活性可能会影响病毒生长的测量的范围。
接下来,该研究评估了剂量反应中确认的已知药物与瑞德西韦之间的潜在协同作用。观察到四种化合物与瑞德西韦具有类似显著的协同作用水平,其中包括汗防己甲素(Hanfangchin A)(也称为粉防己碱(Tetrandrine)),是该研究中验证的两种抗疟药之一(图4c)。 汗防己甲素是一种双苄基异喹啉生物碱,已显示出抑制多个Ca+2通道,并且先前也已报道过它通过靶向内体两个孔通道(TPCs)在体外和体内拮抗埃博拉病毒的进入。但是,氯喹衍生物的细胞抗病毒活性尚未总结在临床试验中,这可能是由于无法达到患者抗病毒活性所需的安全有效浓度。这些数据表明应进一步研究组合方法,以确定两种药物在可接受的安全范围内是否存在体内和临床协同作用。
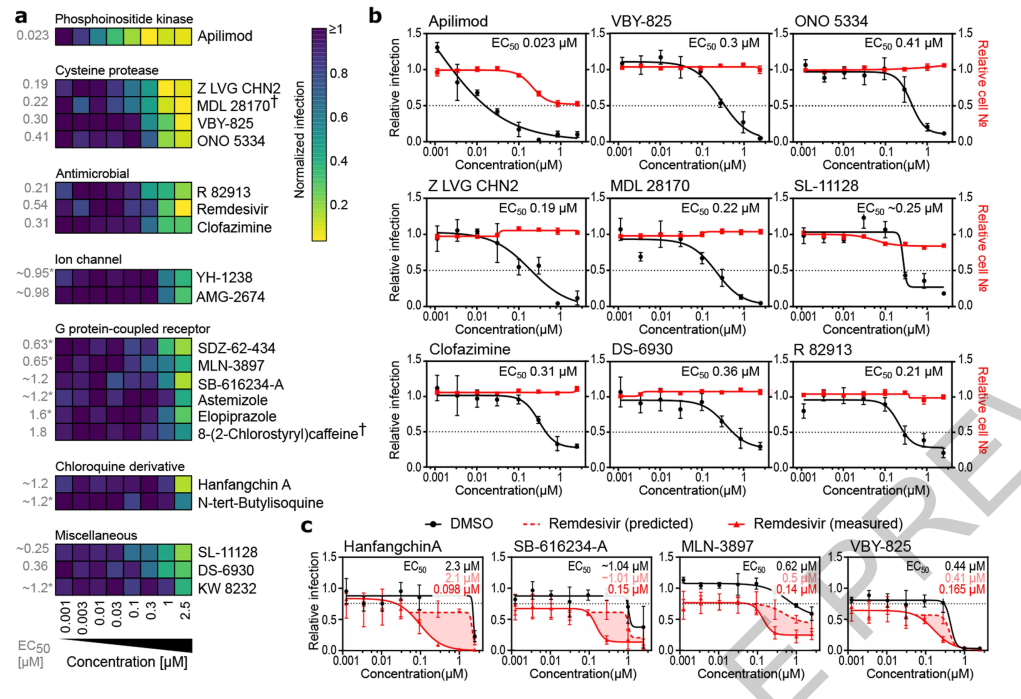
图4:所选抗病毒化合物的剂量反应关系以及与瑞德西韦的协同作用。 (a-c)用递增浓度的所示化合物预处理Vero E6细胞16小时,然后以MOI = 0.01感染SARS-CoV-2。感染24小时后,将细胞固定,并进行免疫荧光成像。对于每种情况,将感染百分比计算为CoV NP染色的感染细胞数与DAPI染色的细胞总数之比。
5. 人类细胞系的验证
该研究试图确保观察到的功效不仅仅限于细胞Vero E6,希望在人类细胞中也能奏效。该研究在支持SARS-CoV-2复制的两种人类细胞系中,评估了21中化合物的功效并得出结论:几乎所有评估的化合物(19/21)在一种或两种细胞系中的抑制病毒复制的效力都等于或大于细胞Vero E6中观察到的效力。至少在一个细胞系中,有13种含有EC50 < 500 nM 的化合物。
6. 抗病毒药对SARS-COV-2生命周期的影响
研究者继续评估了上述鉴定出的最有效的五个化合物,即apilimod,VBY-825,ONO 5334,Z LVG CHN2和MDL 28170是否对病毒生命周期的进入或进入步骤起作用。他们先进行了加药时间的研究,比较了在病毒感染的同时或者在病毒侵入后的2个与5个小时使用该化合物的效果(图5a)。为了进一步证实这些结果,他们同时评估了这些分子对这些带有SAR-CoV-2 S蛋白,MERS S蛋白或VSV G蛋白基于VSV的病毒样颗粒(VLPs)伪型病毒的感染性的影响(图5b)。从这两个研究实验数据中,可以表明这些化合物抑制病毒复制的进入步骤。重要的是,研究发现蛋白酶抑制剂VBY-825、ONO 5334、Z LVG CHN2和MDL 28170对SARS-CoV-2靶向编码的3c样蛋白酶(3CLpro)和木瓜样蛋白酶(PLpro)缺乏有效的抑制活性,说明抗病毒活性是基于对宿主蛋白酶的抑制。
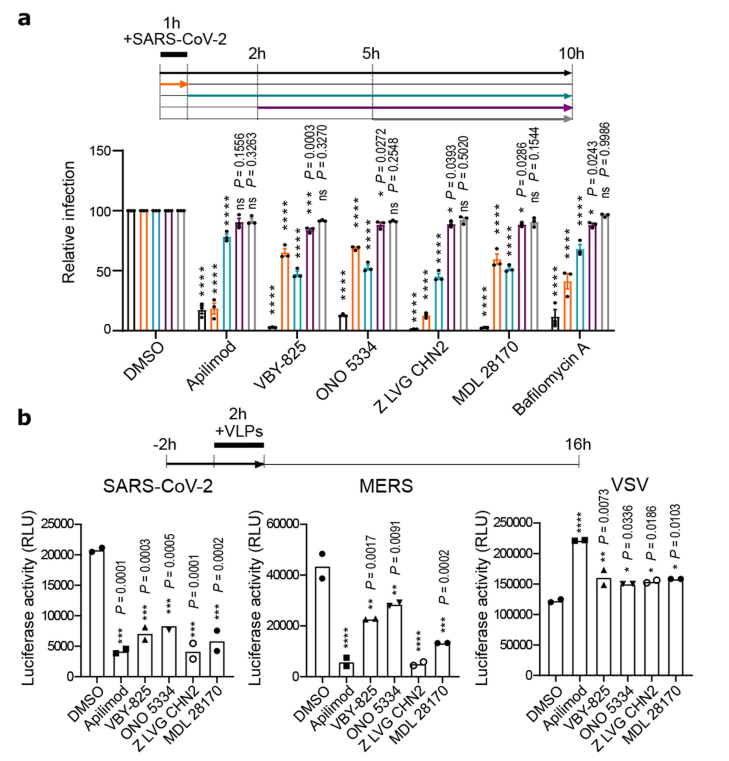
图5:Apilimod和蛋白酶抑制剂可阻止SARS-CoV-2侵入。a: 加药时间的研究;b:病毒样颗粒(VLP)测定。
7. 原代人体细胞模型的评估
研究者进一步评估了ONO 5334,MDL 28170和apilimod在人的多能干细胞(human pluripotent stem cell,hPSC)衍生的肺细胞样的细胞中的抗病毒活性。先分化细胞,然后分别与此三个化合物一起孵育,同时用SARS-CoV-2攻击。抗病毒药物治疗可显著减少病毒在这些原代细胞中的复制。ONO 5334将感染细胞的数量减少了72%(图6a),MDL 28170减少了65%(图6b),而apilimod则阻断了85%的SARS-CoV-2攻击(图6c)。
最后,研究者在体外肺培养系统中评估了apilimod的抗病毒活性。数据表明,apilimod能有效拮抗病毒在组织中的复制,这些组织反映了SARS-CoV-2复制的原发位点。同时也已发现Apilimod在人类中具有良好的耐受性,在≤125 mg BID和峰值血清浓度(Cmax)为0.265 +/- 0.183 µM的剂量下显示出理想的安全性。在合适的动物模型中评估体内功效对于apilimod这个分子作为COVID-19疗法的发展将具有很大的指导意义。
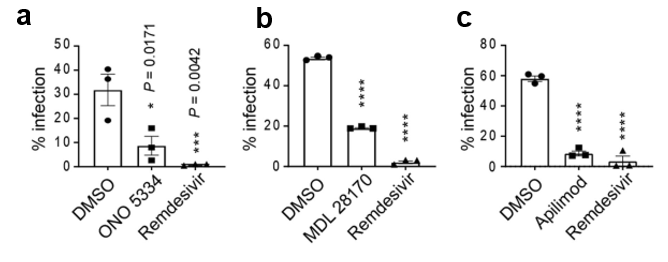
图6:感染前两个小时,将hPSC衍生的肺细胞与5 µM化合物(ONO 5334,MDL 28170和apilimod)孵育,然后感染105 pfu SARS-CoV-2后的实验结果,(a):ONO 5334将感染细胞的数量减少了72%,(b):MDL 28170减少了65%,而(c):apilimod减少了85%。
本文利用生物活性分子库LOPAC作为基准线,高通量筛选已知的分子库ReFRAME,初步得到326个有效化合物,进一步经正交验证筛选得到100种化合物,再经过剂量反应与协同分析筛查出21有效化合物,由EC50< 500 nM标准再筛出13化合物。最后在人的多能干细胞(hPSC)实验中筛查出最有效的三种化合物ONO 5334,MDL 28170和apilimod,其中以apilimod最为有效,安全性也有所保障,但最终仍需体内实验评估(图7)。
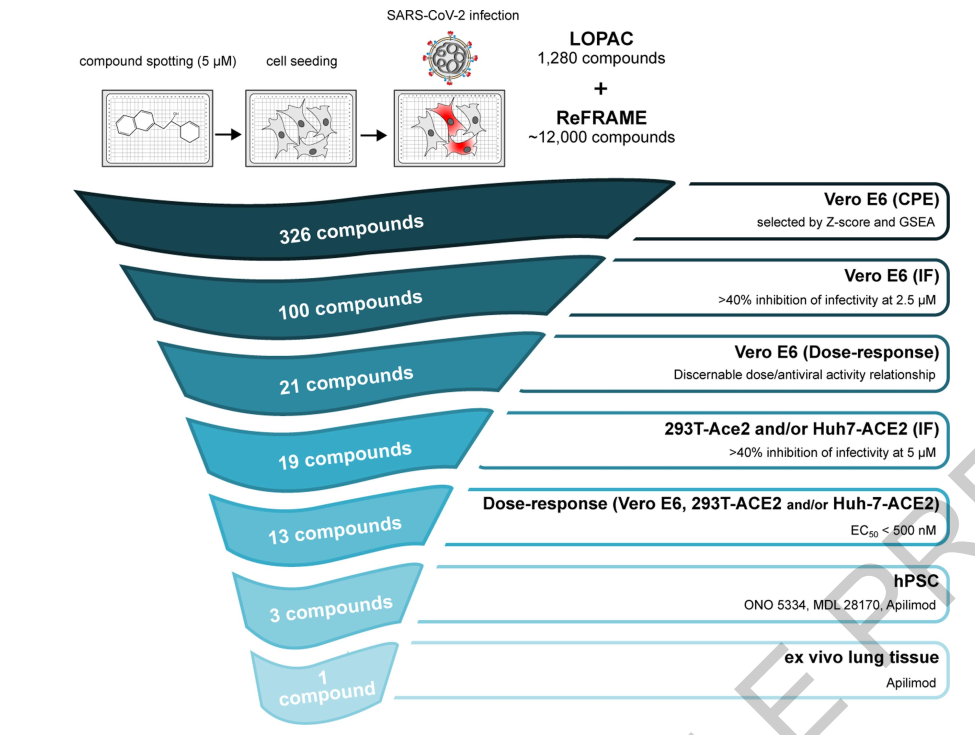
图7:筛选策略和工作流程。概述的显示了本研究的向下选择策略和相应的选择标准
总结
该研究展现了药物筛选的一般过程,对抗病毒的药物研究与发现需要大量的实验与时间,以保证人类在使用药物时有效且安全,药物研发要慎之又慎,而从已知的药物从去寻找治疗新病毒的药物可以保证安全性,并加速药物用于治疗新病毒的临床前和临床评估。
撰稿人:林禄春(博士后)
校稿人:唐永翔(2018级硕士生)