器件小组文献分享
Nature: 定位原子力显微镜

1 前言
在单分子水平上了解生物大分子的结构动力学,对于推进分子机制的了解至关重要。但由于其结构复杂性和动态特性,观察生物分子的天然结构和行为仍是具有难度的。冷冻电子显微镜和X射线晶体成像两种技术的应用,使蛋白质结构的测定进展迅速。然而,这两种测定分子结构的方法,分子被固定在晶体中,或者在超低温下冷冻,这往往会改变它们的正常生理形状。生物大分子在生理温度下的结构是高度动态的。目前,很少有技术可以在亚纳米尺度和生理相关条件下捕获其结构动力学信息。原子力显微镜 (Atomic force microscopy, AFM) 具有在生理缓冲液、环境温度和压力下分析未标记单分子的优势。AFM 可在类似原生环境中对分子进行成像,例如(i)在环境温度下,(ii)在环境压力下,(iii)在生理缓冲液中和(iv)在膜中(在膜蛋白的情况下)。此外,AFM测量机制和流体池的开放性允许在图像采集过程中进行(v)缓冲液交换、(vi)温度变化和(vii)力变化。高速原子力显微镜(High Speed-AFM, HS-AFM)可以实时检测单个生物分子的信息以及更快的扫描和反馈操作,有效地揭示蛋白质的构象变化。然而AFM针尖的尺寸有限,且生物样品是柔软且动态的,其通常不能解析蛋白质表面的亚分子结构特征,分辨率较低。
来自美国威尔康奈尔医学院的George R. Heath等研究者报道了用定位原子力显微镜(localization AFM, LAFM)克服了目前AFM分辨率的限制。定位显微镜方法,也称为超分辨率荧光显微镜。随机光学重建显微镜和光活化定位显微镜 (photoactivated localization microscopy, PALM) ,可以观测到细胞结构和大分子组装。这两种方法通过在图像中以高空间精度隔离和精确定位激发荧光信号的来源,可以重建高横向分辨率图,将由光的衍射极限限制的约400 nm 分辨率极限降低到约20 nm。作者根据荧光定位显微镜方法(图1a-d),开发了LAFM,将定位算法应用于AFM和HS-AFM图像中地形特征的空间波动(图1e-h)。与X射线结构和分子动力学模拟的比较表明,这种方法可以揭示埃米范围高分辨率的蛋白质表面细节。
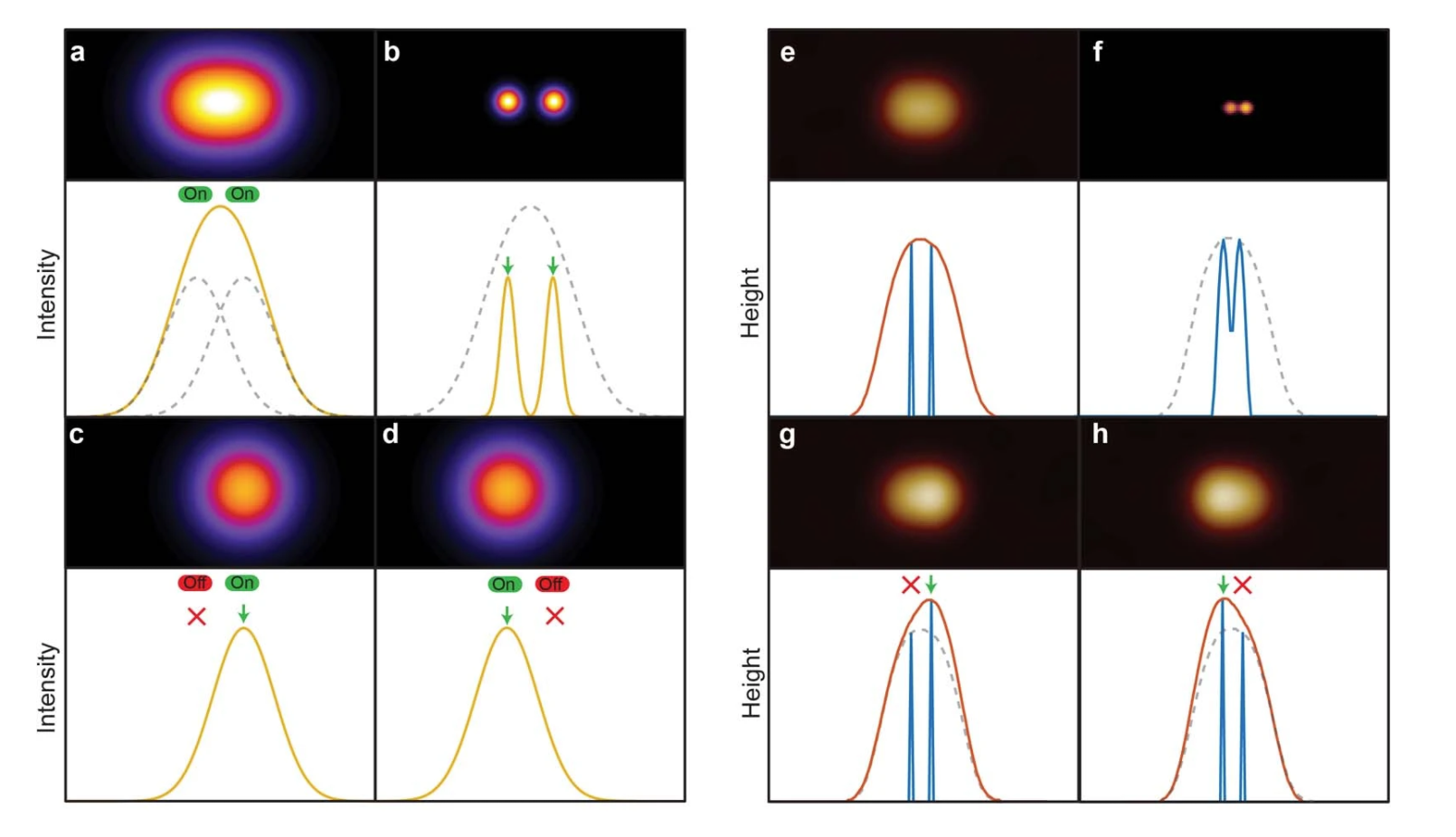
图1. PALM中的定位原理。 (a)位于小于衍射极限的分离距离处的两个荧光分子的衍射极限图像/轮廓。 (b-d)应用PALM后荧光团的空间分辨位置。
2 突破分辨率限制
通常,从顶点到被成像物体尖端几何形状远大于目标特征之间的间隔距离(图2a、b,Surface)。AFM针尖半径的限制会导致在横向上识别目标十分困难,且信号会进一步被z方向的噪声和柔性蛋白质表面特征在x、y、z方向上的随机波动(图2b, AFM traces)所阻碍。对这些轨迹进行平均可以去除噪声并产生无噪声的地形轨迹,但尖端卷积仍然是一个限制因素(图2b,Avergae-AFM)。通过应用检测同一系列轨迹中的局部极大值的定位算法,提取特定位置的高度(图2b,LAFM height),并将单个检测合并到峰概率图中(图2b,LAFM probability)。在LAFM图中,以更大的横向分辨率重建表面结构(图2b,LAFM)。在AFM数据中识别和累计局部极大值的局部峰值搜索算法以前曾被用于创建概率密度图,从中计算出的能量图可以对蛋白质部分的构象空间进行采样,并得出刚度图。在这里,作者利用超分辨率荧光定位显微镜的发展所产生的方法学知识扩展了该方法。当在图像中以较高的空间精度确定孤立信号的定位时,可以获得优于物理限制的分辨率,这些图像随后被合并到地图中,该地图具有比初始数据更高的横向分辨率。它的优点精度很高,可以确定具有宽强度分布的信号的峰值位置。之后作者将这种原理应用于AFM数据。首先,对像素和AFM限制的低横向分辨率数据采样,以提高空间定位分辨率和确定峰值位置。测量峰值位置,然后合并定位数据,得到一个比初始像素采样具有更高横向分辨率的重建地图。
模拟结果表明,LAFM算法可以检测到隐藏在理论和平均拓扑结构中的特征结构(图2b)。在平面样本上时,检测效果最好。当存在相邻的高特征峰时,检测到特征结构概率与突起高度呈非线性关系。之后作者对真实AFM数据进行图像扩展后检测局部高度最大值(图2c)。重建的LAFM地图从许多粒子中编译出由峰值概率细化的平均地形高度,其中每个像素携带关于地形的完整信息及其在该位置被检测的可能性。在合并多个粒子时,随机分布的仪器噪声会被抵消掉,而蛋白质表面波动中出现的峰值检测将合并成高分辨率重构LAFM中的强局部信号。
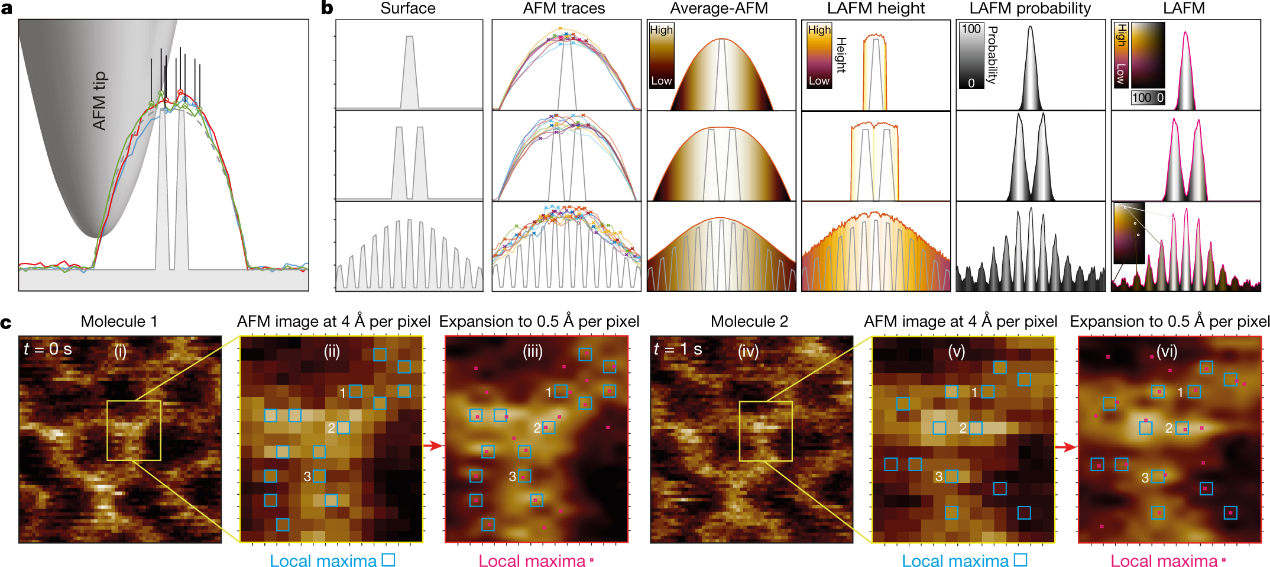
图2. LAFM原理。 (a)AFM针尖扫描高分辨率地形的示意图。虚线,理论等高线。彩色线条,三种具有代表性的模拟地形痕迹。(b)LAFM方法在具有一个(顶部)、两个(中间)和多个(底部)高度调制表面特征的表面上的模拟(n = 1000)。表面:表示理想化的表面特征(灰色)。AFM轨迹:9条具有代表性的模拟地形轨迹(彩色线),检测到局部极大值(叉)。平均AFM:平均形貌(n = 1000)。LAFM高度:检测到的局部极大值的平均高度。LAFM概率:检测到的局部极大值的峰值概率分布。LAFM:用峰值概率合并实空间高度的LAFM映射。(c)高空间分辨率地形局部极大值检测。(i), (iv),两个代表性的序列(t = 0 s, t = 1 s) annexin-V(A5)三聚体的原始数据图像。(ii), (v),放大的原始数据视图(每像素4 Å)。蓝色方块。在两幅图像的相同像素位置检测到标记为“1”、“2”和“3”的局部极大值。(iii), (vi),相同的图像区域后的图像扩展(每像素0.5 Å)。红色方块,局部最大像素。
3 蛋白质表面的单一氨基酸
作者将LAFM应用于传统AFM数据集。在将水通道蛋白-z(aquaporin-Z, AqpZ)四聚体通道提取和对齐后,LAFM图的精度达到了x射线结构表面的水平(图3a),分辨出了表面突出环上的单个氨基酸(图3b)。LAFM 概率图显示了LAFM检测先前隐藏的结构特征(由2.6 Å分隔)的能力,远远超出了先前平均和峰值概率方法(11 Å)以及原始数据的奈奎斯特频率(1/(6.6 Å) ) 。作者还将LAFM方法应用于HS-AFM视频中的A5三聚体(图2d),发现LAFM图可以沿分子主干分辨精细结构细节(而平均的方法只分辨了蛋白质包膜)(图2b)。
为了定量评估LAFM图的分辨率,作者使用了傅立叶环相关(Fourier ring correlation, FRC)方法。FRC方法将数据集分成两半,并以分辨率范围的函数来评估它们的统计相似性。通过该分析得到,AqpZ的分辨率为4.0 Å,A5的分辨率为5.1 Å(图2c,f)。AqpZ的FRC曲线在2-Å范围内同样包含信息。所以,AqpZ LAFM半图的统计分析报告的分辨率低于原始数据的奈奎斯特频率。因此,AqpZ和A5的LAFM图谱可以分辨氨基酸大小范围的细节(大约5 Å到4 Å),在AqpZ的情况下,可以在准原子尺度(大约2 Å)上得到一些信息(图2b, c)。
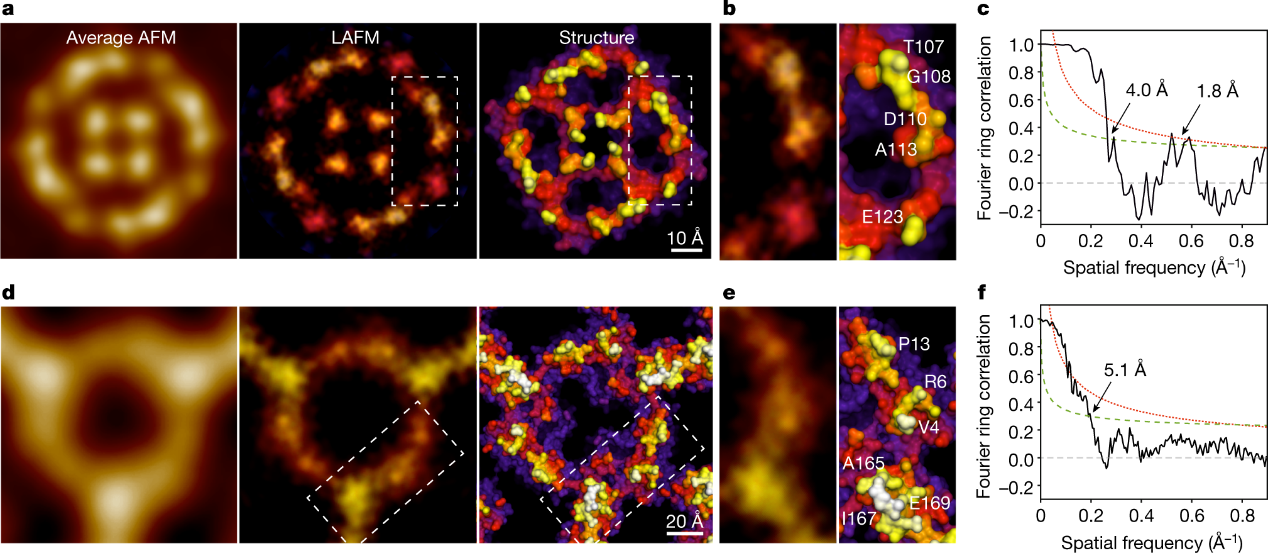
图3 . AqpZ和A5的LAFM。 (a-c), AqpZ; (d-f), A5。(a, d),左,平均AFM图;中间,LAFM地图;右边是x射线结构的表面表示。(b, e), LAFM图和x射线结构的详细视图,标记了可识别的残基。(c, f), FRC分析的LAFM半映射。
4 CLC对映体的原子力显微镜定位
文章还研究了CLC-ec1(chloride channel-ec1,氯化物通道),AFM目前尚未能观察到这种物质,其转运机制有待探究。
CLC-ec1的HS-AFM图上显示在蛋白质-脂质体融合形成的膜上有一个蛋白分散群体,且其从膜上凸出1.2 nm(图4a-c)。CLC-ec1主要是二聚体、少量单体以及由多个二聚体组装的高阶低聚物(图4b)。二聚体的外形和尺寸(图4c)与CLC-ec1外表面的5.5 nm× 9.6 nm的尺寸(图5a-e)是一致的。
由于二聚体可以表现出平移和旋转的特性,该文章提出了一种广义的LAFM测量方法(图4d):1.获取HS-AFM图像;2.低通滤波;3.自动检测粒子;4.在整个观测过程中粒子被追踪;5.粒子在图库中被选取;6.双三次插值算法扩展图像;7.精确粒子中心化;8.与任意分子旋转对齐;9.1.第二次横向排列;9.2.第二次旋转排列;10.1.检测局部最大峰值;10.2.以1.4Å为概率半径提取;11.最终所有的检测结果合并到高度-概率的LAFM图中。
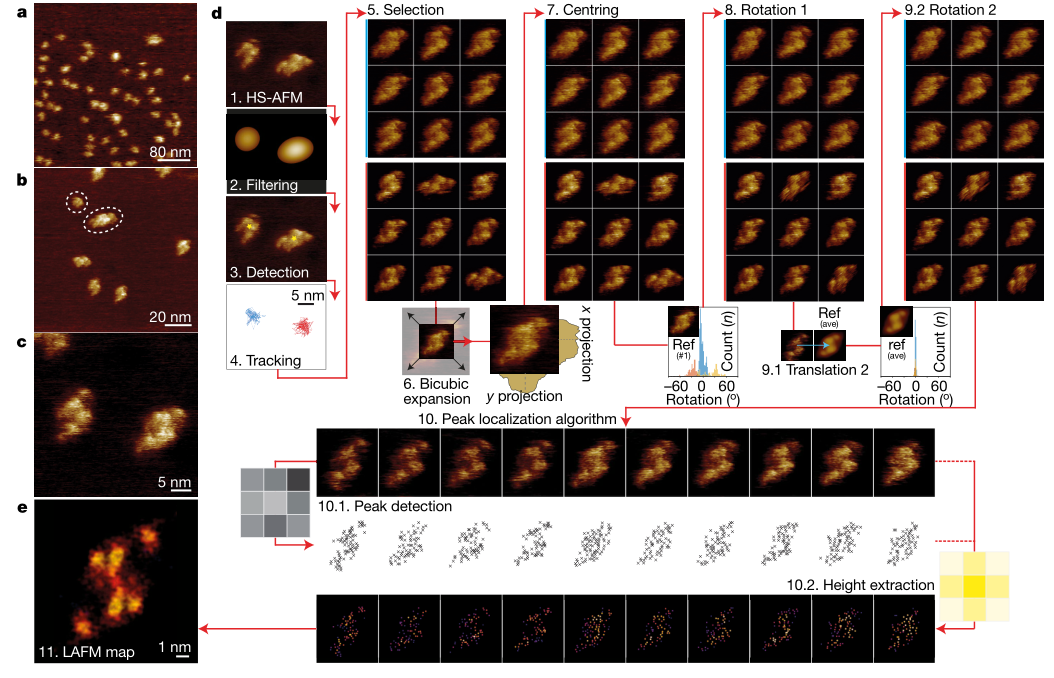
图4 HS-AFM成像和CLC-ec1检测的LAFM工作流程。(a-c),CLC-ec1在400 nm膜上的HS-AFM成像(300像素);(a),120 nm(300像素);(b),40 nm(300像素);(c),以二聚体为主的CLC-ec1在低密度膜中的图像;(d),LAFM工作流程。
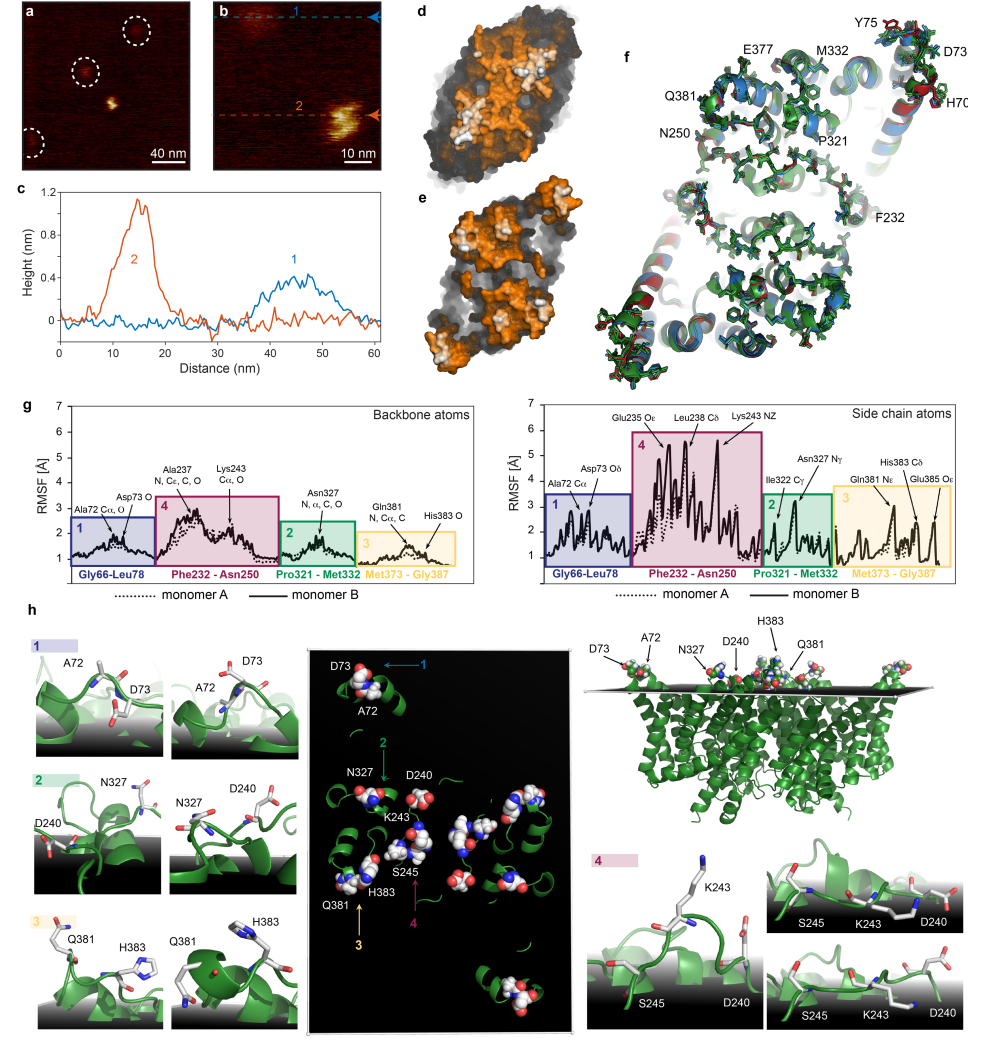
图5 CLC-ec1的细胞外侧。(a),(b),HS-AFM视频,CLC-ec1在双分子层中:检测到仅突出一点点的分子和突出较远的S形分子。(c),(b),中所示的两个分子的剖面分析:一个分子种类仅从双分子层中突出4Å,而CLC-ec1的S形分子从膜表面突出11Å。(d),(e),X射线结构的细胞内(d)和细胞外(e)的表面。根据结构比较,将S形的CLC-ec1 HS-AFM拓扑图分配给细胞外表面。只有S形胞外面的分子被整合到LAFM分析中。
5 CLC-ec1的构象变化
在CLC-ec1 Cl-/H+-反向转运蛋白中,转运途径是在细胞内有两个独立的H+和Cl-的入口/出口,离子通过该途径汇聚到同一个中心结合区,然后沿着相同的路径进入细胞外侧。然而关于该“门控机制”是否仅仅发生了由 X射线所发现的Cl-通路中的侧链运动,还是发生了更大的运动?目前尚未得出结论。
一些非晶体学方法发现由于三维晶格中的限制而抑制了CLC大的构象运动(图5f), 质子化模拟的三重突变体的最新结构也表明其构象上的重新排列。因此,该文章对疏散在脂质膜中的运输体使用HS-AFM进行了观测,分别在pH7.6(非活性状态)和pH4.5(活性状态)状态下进行了观察。
在X射线结构表面的基础上(图6a),文章标记了预计会在AFM中产生信号的突出残基:B-C环的Asp73、I-J长环的Glu235、Asp240和Lys243、L-M环的Asn327以及N-O环的Gln381和His383。同时为了补充完善LAFM的解释,作者还使用了分子动力学模拟,将静态的X射线结构转换成动态的分子结构,绘制了CLC-ec1细胞外表面Z坐标局部极大值分布的群体密度图,该图反映了膜突起的侧链运动。(图6b,图5g,h)。分子动力学轨迹显示出结构波动是如何被探测到的以及是如何从合并的结构波动中提取高分辨率下的蛋白质表面的氨基酸残基的信息。
CLC-ec1在pH7.6和pH4.5时的LAFM重建图像显示出与X射线结构和分子动力学模拟图相同的结构特征,但得到的图像却发生了变化(图6c,d)。峰2、3和4在二聚体界面附近形成一个三角形。在pH4.5时,它们则更加松散,峰3向更侧边的位置移动,而最显著的构象变化是峰1在酸性pH条件下向二聚体界面移动了约6Å。如图6c中“*”号部分所示,细胞外Cl-/H+离子通道位于Asp73、Asn327和Glu235之间;因此,在这些位移与底层螺旋的运动有关的前提下,这些结构的变化可能会改变细胞外门的可及性。综上所述,LAFM图像显示了较大依赖于pH值的构象变化(图6e)。
根据CLC-ec1在不同pH值下的成像计算出的LAFM图,确定了中心区域产生差异的原因,即螺旋N和O所在的区域,以及在螺旋B的外围端向二聚体中心移动,使整个分子呈现出约1.2nm的缩短。(图6d,e)
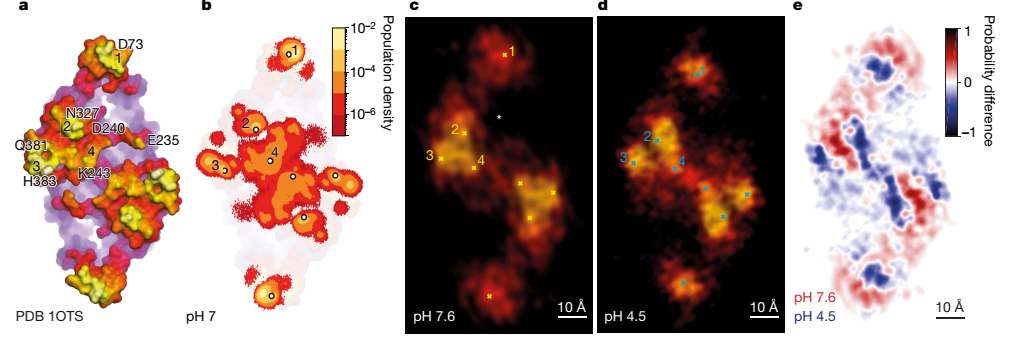
图6 CLC-ec1在中性和酸性pH下的构型变化。(a),pH值9.5条件下的CLC-ec1的细胞外表面;四个主要突起(1-4)中的残基被标记。(b),对数尺度的原子位置密度图。 细胞外表面Z坐标最高的原子位置的对数尺度群体密度图,该图来自在pH值为7时5.6 ms的分子动力学模拟结果。主要的突起(1-4)被标记为对每个群体峰值的贡献值:(1)D73(97%),A72(2.7%);(2)N237(91%),D240(2.2%);(3)Q381(42.3%),H383(54.7%);(4)K243(52%),D240(21.7%),S245(3.4%)。(c),(d),CLC-ec1在pH 7.6(c)和pH 4.5(d)的LAFM重建图像。离子通路入口用星号标出。四个主要的突起(1-4)被突出显示,以便与X射线结构和分子动力学模拟的群体密度图进行比较。(d),在pH7.6(c)和pH4.5时CLC-ec1 LAFM重建的差异图,差异图突出了四个主要突起的构象变化。特别是峰1向二聚体轴线移动了约6-Å。(e),在pH为7.6和4.5时,CLC-ec1 LAFM重建之后的差异图。
总结
HS-AFM在振幅调制模式下工作,尖端只在大约10%的振荡周期中接触到表面,大约为150 ns。尽管相对蛋白质的生命而言,这是一个很短的时间段,但侧链的波动如果发生在这样的时间段内会使信号模糊。因此,当下一代更快的HS-AFM系统到来之前,LAFM将提供更好的数据。总之,该文章提出的LAFM将成为应用于原子力显微镜成像的标准方法,其可以在类天然环境中单个生物分子的研究中提取超出AFM针尖半径分辨率极限的高分辨率信息。
原文地址:https://www.nature.com/articles/s41586-021-03551-x#Sec3
撰稿人:赵骄阳(2020级硕士生)
校稿人:刘文清(2020级硕士生)